首页>技术中心>技术资讯>水的采样和化学性质分析――磷的测定
水的采样和化学性质分析――磷的测定
发布时间:2017-09-01
1、 分析意见
雨水天然水中磷含量通常很低,一般每升中仅数十微克。但近年来随着含磷化肥施用量不断增加,以及含磷洗涤剂的使用,使磷随雨水或污水排入江河湖泊,使水体中磷不断富集。水中磷主要以各种磷酸盐的形态存在,也有由于生物化学过程产生的有机磷化合,通过测定水中磷和无机磷含量可估计水体是否污染以及污染的程度,是判断水质富营养化的重要指标。
2、 方法选择的依据
磷的测定多用磷钼蓝比色法,但水样中有机磷需经氧化分解转化成正磷酸盐才能显色而用钼蓝法比色。有机磷的氧化,多将水样蒸干,加入硫酸、高氯酸(或过氧化氢)加热,将有机磷转化成正磷酸盐然后用钼蓝比色法测定。近年来,也有将水样中加入过硫酸钾在高压条件下氧化将有机磷转成正磷酸盐然后用钼蓝比色法测定。水中无机磷可直接用钼蓝法比色。
3、 硫酸-高氯酸氧化-钼蓝比色法
(1)方法原理
水样经蒸干后,用硫酸和高氯酸(或过氧化氢)氧化,使水样中各种形态磷转化成正磷酸盐,溶液中的正磷酸根在适当的酸度和还原剂的存在下与铂酸形成磷相杂多酸而显蓝色,用分光光度法测定其吸收值,并在磷的工作曲线上查出磷的浓度,从而计算水中总磷的含量。水中无机磷可直接显色比色侧定。
(2)仪器及设备
可控温电炉;分光光度计。
(3)试剂
①硫酸(H2SO4p=1.84g・cm-3,分析纯);
②高级酸(HCIO4,p=1.60g・cm-3,分析纯);
③二硝基酚指示剂:称取0.2g2.4-二硝墓酚或2.6-二硝基酚指示剂,加水溶解稀释至100 mL;
④氢氧化钠溶液[c (NaOH)=10mol・L-1],40g氮氧化钠(NaOH,分析纯)溶于水稀释至100 mL;
⑤稀氢氧化钠溶液[c(NaOH)=0.1mol・L-1〕:将上述氢氧化钠溶液(试剂4)稀释至100倍;
⑥硫酸溶液[c(二分之一H2SO4)=0.1mol・L-1]:取浓硫酸0.3mL注入100 mL水中;
⑦钼酸铁-硫酸溶液:称取25g钼酸按[ (NH4)6Mo7O24・4H2O,分析纯)溶于300 mL温水中(水温不得超过60℃),另取280 mL硫酸(试剂1)慢慢倒入400 mL水中,冷却后将硫酸溶液倒入钼酸铵溶液中,边倒边搅拌,最后定容至1L;
⑧氯化亚锡溶液:称取2.5g氯化亚锡(SnCl2・2H2O,分析纯)溶于100 mL甘油(又名丙三醇,〔CH3H5(OH)3],化学纯}中,并在沸水浴上加热溶解,此液可能会有少且混浊,但不影响使用,贮于棕色瓶中于暗处保存,可长期使用。
⑨磷标准贮存溶液:[p(P)=100mg・L-1]:称取50℃洪干4h的磷酸二氢钾(KH2PO4,分析纯))0.4390.g,溶于少量水中,洗入1000 mL容量瓶,加入浓硫酸(试剂1) 5mL,定容至刻度摇匀。可长期保存。
⑩磷标准溶液[p(P)=5mg・L-1]:吸取确标准贮存溶液(试剂9)25mL定的500 mL容量瓶中。此液不宜久存。
(4)操作步珠
①吸取水样25-100mL(含P1μg~10μg)于100mL烧杯中,加硫酸(试剂1)1mL在电炉上低温蒸干,至近干(硫酸微发烟)时取下冷却,沿烧杯壁滴加高氯酸(试剂2)1mL,在电炉上加热使硫酸发烟赶尽高氯酸,取下冷却,洗入25mL容11瓶(如有沉淀需过滤)。加水20 mL左右,加1滴二硝基酚指示剂(试剂3)用氮氧化钠溶液(试剂4,试剂5)及硫酸溶液(试剂6)调节至微黄色,加1mL相酸铵-硫酸溶液(试剂7)定容摇匀。再加2滴氯化亚锡甘油溶液(试剂8)摇匀。放置5min~15min(室温200C以下为15min,200C~300C为8min,300C以上5min)在分光光度计上比色,用660 nm波长3 cm比色皿。读取吸收值,在工作曲线上查得磷浓度。
②工作曲线侧定:吸取磷标准溶液(试剂10)0mL,0.5 mL,1.0 mL,1.5 mL,2.0 mL,2.5mL,分别于25mL容量瓶中按样品测定同样调pH。显色、比色并绘制工作曲线。
(5)结果计算
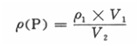
式中p(P)――水样中总磷含量,mg・L-1;
P1――在工作曲线上查得显色液中磷的浓度,mg ・L-1;
V1――显色液定容体积.mL ;
V2――吸取水样体积,mL。
(6)注意事项
①氯化亚锡比色法对溶液酸度、显色温度以及显色后放置时间要求较严,一定按方法要求操作。
②如水样中含磷过低,显色后蓝色很浅,直接比色有困难时,可显色后用异丁醇萃取后比色。
参考资料:土壤农业化学分析方法







