首页>技术中心>技术资讯>EDTA与金属离子的配位化合物(四)
EDTA与金属离子的配位化合物(四)
发布时间:2017-09-01
五、考虑其他副反应时的配合物的条件(稳定)常数
1、配位化合物的条件稳定常数
在研究EDTA滴定实际反应体系时,应考虑副反应的存在,将反应式写成:
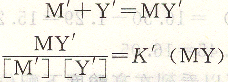
K’MY称条件稳定常数,简称条件常数,表示在有副反应存在时配位化合物反应进行的程度,K’MY是KMY经副反应系数校正后配位化合物反应的实际稳定常数。
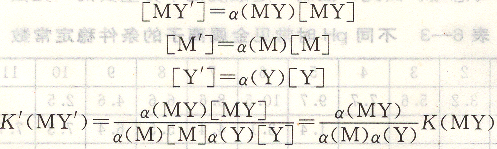
在一定条件下(如介质pH、试剂浓度)a(M),a(Y),a(MY)均为定值,因此K’(MY)在一定条件下是个常数,它是随条件而变的,也称为表现稳定常数或有效稳定常数,见表6~3。
条件稳定常数对数形式表示式为lgK’(MY)=lgK(MY)一lga(M)+lg (Y)+lgd(MY)多数情况下,不考虑MHY或MOHY,lgK’(MY) 简化成:
lgK’(MY)=lgK(MY)一1ga(M)一lga(Y)
这是常用的配位化合物条件常数的重要公式。
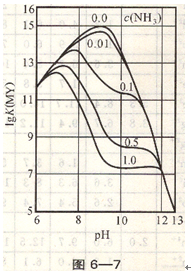
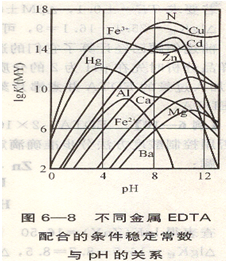
仅仅考虑酸效应的影响,可以看到在高酸度下配位化合物反应是不完全的。由图6―5与图6―61gay(H)-pH曲线中也可以知道,低酸度条件下虽然酸效应系数较小,但金属离子的反应不可忽略。因此,控制一定酸度是十分重要的(见图6―8)。
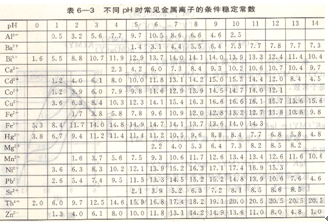
配位化合物条件稳定常数在配位化合物滴定中用于计算化学计量点pM、指示剂选择与滴定误差、滴定介质pH选择以及单一离子、混合离子滴定可行性的判断。配位化合物平衡计算最终是lgK’(MY)计算,这必须涉及求算副反应系数,所以说副反应系数法是处理复杂配位平衡的简单实用方法。
2、混合离子连续滴定可行性判断界限与控制酸度的分步滴定
混合离子连续分步滴定是EDTA滴定的重要应用。实现连续滴定的方式是多种的,如控制酸度pH在2,3,5,10;介质分别以磺基水杨酸、PAN为指示剂,连续分步滴定测定Fe3+,Al3+,Mn2+, Mg2+。如采用仪器指示法,在每次测定之后提高pH,可以实现V(Ⅲ)一V(Ⅳ),Fe3+一Mn2+,Ca2+一Cu2+,Br3+―Pb2+―Ca2+,Cu2+一Ni2+,Ni2+一Zn2+,Cu2+一Zn2+一Ca2+的安培滴定;采用双指示剂光度指示法实现Ca2+- Mg2+,Zn2+-Mg2+,Bi2+一Pb2+,Cu2+一Zn2+,Fe3+一Mn2+ 。采用掩蔽与选择性解, Pb2+可在Zn2+、Cd2+存在下用KCN掩蔽、甲醛解蔽的方法实现连续测定;采用选择性EDTA释出法可测定Pb2+一Hg2+-Tl3+、Fe3+―Al3+―T13+。
实现连续分步滴定是基于EDTA与金属离子配位化合的稳定性差别。若△Pm=±0.2,T.E=±O.1%,且cm=cn,则△lgK稳≥6,可以实现分步滴定。
正如单一离子滴定可行性判断界限那样,由于目测点与化学计量pM点的差值,△pM在±O.2~±0.5,T.E>0.1%。实际判断可否准确滴定,与对△1gK稳、T.E、△pM的要求有关。这里学习的仅是处理此类问题的方法,不再进一步讨论更复杂的体系,因为实际测定中还是通过实验来选择适宜的pH。
参考资料:分析化学







