首页>技术中心>技术资讯>EDTA与金属离子的配位化合物(三)
EDTA与金属离子的配位化合物(三)
发布时间:2017-09-01
四、考虑其他副反应时的副反应系数
配位化合物滴定中涉及的化学平衡比较复杂,不能像酸碱反应那样,单靠引入分布系数、分布系数图来解决所涉及的平衡组分计算。以EDTA配位化合物滴定为例:
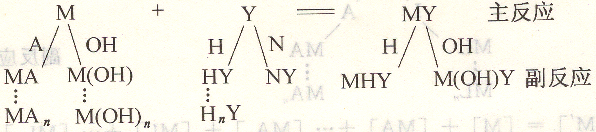
除M与Y之间生成MY的主反应外,将受介质pH、其他共存金属离子(N)以及配合剂(A)的影响发生其他反应,这类反应统称为副反应。它将影响主反应进行的程度,影响主反应组成及生成物的浓度。用副反应系数定量描述副反应对主反应的影响程度。
1、滴定剂Y的副反应及副反应系数αy
(1)EDTA酸效应与酸效应系数ay(H)
(2)共存离子效应
除金属离子M与Y生成配位化合物反应外,共存金属离子N也与Y生成配合物,反应称为共存离子效应,是滴定剂Y存在的副反应,用副反应系数ay(H)表示。
(3)滴定剂Y的总副反应系数aY表示。
aY= ay(H)+ ay(n)―1
滴定剂副反应系数虽然有几项,我们讨论的滴定中仅考虑ay(H)一项。
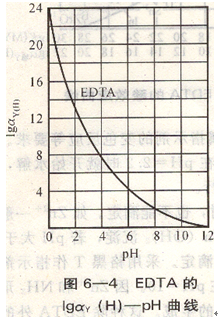
对于酸效应系数我们仅做理论上的了解,搞清是怎样计算出来的即可,在实际应用中可查表得到。由lgay(H)-pH表6-2,了解lga ay(H)随pH变化的趋势,滴定介质pH越低,酸度愈高,酸效应系数愈大,影响愈大。
2、金属离子的副反应及副反应系数
由于其他配合剂(L或A)存在,使金属离子(M)参加主反应的能力降低的现象称为金属离子的副反应,其副反应系数用a(M(L))表示。
a(M(L))表示金属离子总浓度[M,]是游离金属离子浓度[M]的多少倍。
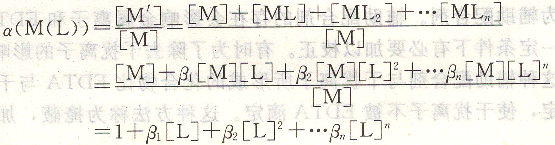
可见,a(M(L))仅是[L]的函数。
溶液中金属离子因介质pH可形成羟基配合物,溶液中存在的辅助配合剂、掩蔽剂,缓冲溶液组分都可能与金属离子生成配位化合物,发生多种副反应。此时应当用金属离子总副反应系数a(M)表示。若溶液中有两种配合剂L和A同时与金属离子M发生副反应。
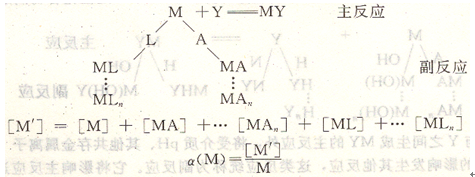
对初学者来说,无需对n种配合剂发生的多个副反应进行重复计算,只需从两种副反应即a(M)=a(M(L))+a(M(A))-1人手,掌握用副反应系数方法处理复杂的配位化合物平衡即可。
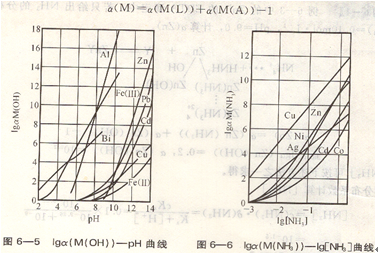
在水溶液中,当溶液酸度较低时,金属离子生成多种羟基或多核羟基配位化合物,以a(M(0H))表示(见图6―5)。在配位化合物平衡计算中,溶液酸度是必需考虑的因素,a(M(OH))可由附录中附表5查得。
3、配位化合物MY的副反应及副反应系数
配位化合物MY在酸度较高时,能生成MHY,使EDTA对M的总配合能力增强;配位化合物MY在酸度较低时能生成MOHY的副反应,同样增加EDTA对M的配合能力,这种副反应分别以副反应系数a(MY(H))、a(MY(OH))表示
MY+H=MHY
MY+OH=MOHY
由于MHY及MOHY大多不太稳定,一般忽略不计。
参考资料:分析化学







