水样中氯含量的测定――莫尔法
发布时间:2017-09-01
一、目的要求
1、掌握莫尔法测定氯离子的方法和原理。
2、巩固以K2CrO4为指示剂判断终点的方法。
二、实验原理
水中氯含量的测定通常采用莫尔法。该方法是在中性或弱碱性溶液中,以K2CrO4为指示剂,用AgNO3标准溶液滴定。其滴定反应为:
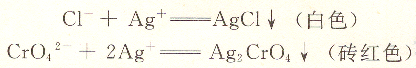
根据分步滴定的原理,由于AgCl的溶解度比Ag2CrO4小,因此在计量点前首先析出AgCl沉淀,当达到计量点时,CI-已定量沉淀完全,过量1滴AgNO3溶液就与CrO42-离子结合生成砖红色的Ag2CrO4沉淀,从而到达指示终点。
滴定只能在中性或弱碱性溶液中进行。若酸度过高,由于Cr042-离子浓度降低,不利于生成Ag2CrO4沉淀。
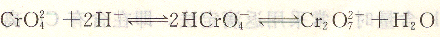
若酸度过低,则Ag+与OH一生成Ag2O沉淀。

本法滴定的适宜pH范围为6.5~10.5。如果有铵盐存在,则溶液的pH需控制在6.5~7.2之问。
三、实验试剂
1、0.1mol・L-1AgN03标准溶液;
2、自来水。
四、实验步骤
准确量取50.00mL自来水于250mL锥形瓶中,用lmL吸量管加入lmL5%K2CrO4溶液,在充分摇动下,用AgNO3。
标准溶液滴定至呈砖红色即为终点。平行测定3次。
五、结果计算
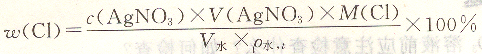
式中:c(AgN03)――AgNO3溶液的浓度,mol・L-1;
V(AgNO3)――AgNO3溶液的体积,mL;
M(C1)――Cl的摩尔质量,g・mol-1;
V水――自来水的体积,mL;
P水,t――t℃时自来水的密度,kg・L-1。
参考资料:分析化学







