混合离子的分别滴定(二)
发布时间:2017-09-01
使用掩蔽剂时需注意以下几点:
①掩蔽剂应不与待测离子配位,即使能生成配合物,其稳定性也应远小于待测离子与EDTA配合物的稳定性。
②掩蔽剂与干扰离子形成的配合物不仅应远比与EDTA形成的配合物稳定,而且形成的配合物应为无色或浅色,不影响终点的判断。
③使用掩蔽剂时应注意适用的pH范围。例如在Ph=8~10时测定Zn2+,用铬黑T作指示剂,则用NH4 F可掩蔽Al3+。但是在测定.Mg2+、Ca2+和A13+溶液中的Mg2+、Ca2+总量时,在Ph=10滴定,因为F-与被测物将会生成CaF2沉淀,故不能用氟化物来掩蔽Al3+。
④使用掩蔽剂时还要注意其性质和加入时的pH条件是否合适。例如,KCN是剧毒物,只允许在碱性溶液中使用;掩蔽Fe3+、Al3+等的三乙醇胺,必须在酸性溶液中加人,然后再碱化,否则Fe3+将会生成氢氧化铁沉淀而不能进行配位掩蔽。
4、沉淀掩蔽法
在体系中加入一种沉淀剂,使其中的干扰离子浓度降低,在不分离沉淀的情况下直接进行滴定,这种方法称为沉淀掩蔽法。例如,测定Mg2+、Ca2+含量时,由于IgKcaY=10.7,1gKMgY=8.7,△lgK<5,不能用控制酸度的方法分别滴定。但它们的氢氧化物溶解度相差较常用的沉淀掩蔽剂见表4-5。
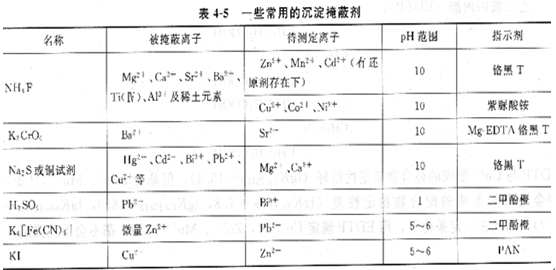
由于一些沉淀反应进行的不够完全,特别是过饱和现象使沉淀不易析出;发生沉淀反应时,通常伴随共沉淀现象;沉淀会吸附金属离子指示剂,从而影响终点观察;一些沉淀颜色深、体积庞大而妨碍终点的判断。因此在实际工作中,沉淀掩蔽法用得不多。
5、氧化还原掩蔽法
利用氧化还原反应,使干扰离子的氧化值发生改变而消除其干扰,这种方法称为氧化还原掩蔽法。例如,测定锆铁中的锆,由于锆和铁的EDTA配合物的稳定性相差不大(△1gK=lgKzrY2-―lgKFeY一=29.9―25.1=4.8<5),Fe3+会干扰锆的滴定。若加入抗坏血酸或盐酸羟胺将Fe3+还原为Fe2+,由于Fe2+-EDTA配合物的稳定常数(1gKfeY2-=14.33)比Fe3+-EDTA配合物的稳定常数小得多,因此,Fe2+不干扰锆的测定。
常用的还原剂有抗坏血酸、盐酸羟胺、硫脲、联氨等,其中有些还原剂同时又是配位剂。例如,Na2 S2 03可将Cu2+还原为Cu+,并与cu+配位。
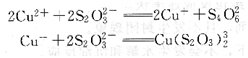
有些高氧化值状态的干扰离子与EDTA不发生配位反应,可以通过将低氧化值状态的干扰离子氧化成高氧化值的方法来消除干扰。例如Cr3+对配位滴定有干扰,但CrO2-4、Cr2 O2-7;则对滴定没有干扰。
6、选择其他配位剂滴定
除了EDTA外,其他氨羧类配位剂与金属离子形成配合物的稳定性也各有特点,可以选择不同配位剂进行滴定,以提高金属离子滴定的选择性。
乙二胺四丙酸(EDTP):
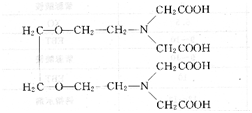
EDTP与Cu2+形成的螯合物稳定性很好(1gKcu-EDTP=15.4),但是与Zn2+、Mn2+、Cd2+等金属离子形成的配合物稳定性差(1gKcu-EDTP= 7.8,1gKcu-EDTP=6.0,1gKcu-EDTP =4.7),因此在一定条件下,用EDTP滴定Cu2+时,Zn2+、Mn2+、Cd2+都不会干扰测定。
参考资料:分析化学







