配位滴定法――概述(一)
发布时间:2017-09-01
以形成配位化合物的反应为基础的滴定分析方法称为配位滴定法。目前,采用配位剂直接和间接测定金属元素的方法,已经日益广泛。本章着重讨论EDTA配位滴定的反应条件、指示剂及有关的基础知识。
一、配位化合物
由一个简单阳离子和几个中性分子或其他离子以配位键相结合而形成的复杂离子叫做配位离子,含有配位离子的盐叫做配位化合物(简称配合物)。例如K4[Fe(CN)6],NH4[Cr(NH3)2(cNS)4],[Cu(NH3)4]SO4等都是配位化合物。
配位化合物一般可以分为内界和外界两个组成部分,内界称为配位离子。它由中心离子和配位体组成,位于配位离子中心的带有正电荷的离子称中心离子,它是配位离子的形成体。中心离子绝大多数是金属离子,如Fe2+,Cr3+,Cu2+,Pb2+,Mg2+等。同中心离子结合的中性分子或离子称为配位体,如:NH3,CN一,CNS-,一COOH,H2O等都是配位体。在配位体中直接和中心离子配位键相结合的原子称配位原子,如NH3中的氮原子、CN一中的氮原子、H2O中的氧原子、一COO*H中带*号的氧原子,都是配位原子。
如:以NH4[Cr(NH3)2(CNS)4]为例说明配位化合物的结构。

与中心离子相结合的配位原子的总个数,叫做中心离子的配位数。
中心离子Cr3+的配位数为2个NH3分子中的氮原子加4个CNS-中的氮原子,总个数为6。一个配位体中具有两个以上的原子直接和中心离子以配位键相结合,则这配位体称多基配位体。如,Ni2+与乙胺配位化合时,乙二胺中有2个配位原子和中心离子Ni2+结合,所形成环状配位化合物称为螯合物,又叫内配位化合物。
配位化合物中配位原子和中心离子之间的配位键用符号“→”表示,说明配位键的孤对电子由配位原子提供,配位原子和中心离子共用。
螯合物的环上有几个原子,就被称为几原子环的螯合物。如:
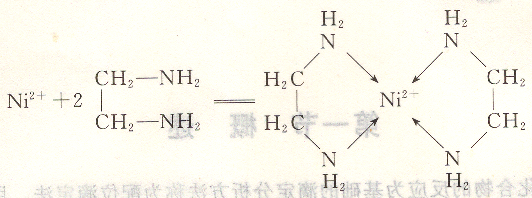
螯合物环上有5个原子,所以称5原子环。螯合物由于有环状结构,比简单配位化合物的稳定性大得多,其中5原子环和6原子环最稳定。同时,由于螯合结构很少有分级解离的现象,因此,此类配位化合物目前在分析化学中是应用最广的。
二、配位滴定反应必须具备的条件
(1)配合反应必须迅速,并生成足够稳定的配位化合物;
(2)反应必须按一定的化学反应式定量地进行,即生成配位数固定的配合物;
(3)要有适当的方法来指示或确定终点,如硝酸银和氰化物的配合反应:

反应能迅速形成稳定的[Ag(CN)2]一配位离子,能定量地形成固定的配位数为2的配合物,当达到等量点时,稍过量的Ag+就会与[Ag(CN)2]一配位离子结合形成Ag[Ag(CN)2]白色沉淀,从而确定终点。其反应为:
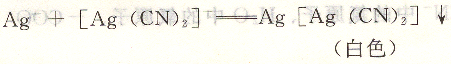
故此反应符合配位滴定对反应的要求,可采用硝酸银标准溶液滴定溶液中的氰化物,根据硝酸银标准溶液用量来计量氰化物的含量。
参考资料:分析化学







