副反应系数和条件稳定常数(二)
发布时间:2017-09-01
三、金属离子的副反应及副反应系数
1、辅助配位效应与配位效应系数
溶液中若存在其他辅助配体L时,而L能与M形成配合物,则M与Y的主反应将会受到影响。这种由于其他配位剂的存在使M参加主反应能力降低的现象称为辅助配位效应。
配位效应的大小用配位效应系数aM(L)表示。
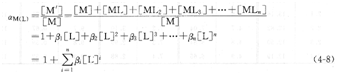
aM(L)越大,则金属离子M与辅助配体L的副反应越严重。如果体系中金属离子M没有发生副反应,则aM(L)=1。附表7列出了部分金属配合物的累积稳定常数。
在配位滴定中,配位剂L可能是滴定条件所需的缓冲剂或者是为了防止金属离子水解所加的辅助配位剂,也可能是为了消除干扰而加入的掩蔽剂。例如,pH=10.0时,用EDTA滴定Zn2+,加入NH3-NH4Cl缓冲溶液,一是为了控制滴定所需要的pH,另一方面使Zn2+生成[Zn(NH3)4]2+,防止Zn(OH)2沉淀析出。
2、羟基配位效应与配位效应系数
在高pH值下滴定金属离子时,金属离子与OH一生成各种羟基化配离子,这种现象称为金属离子的羟基配位效应,也称为金属离子的水解效应,此时的羟基配位效应系数用aM(oH)表示。附表8中列出了部分金属离子的aM(OH))值。
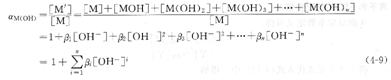
3、金属离子的总副反应系数
若溶液中金属离子存在以上两类副反应:羟基配位效应和辅助配位效应,则金属离子的总副反应系数可用aM表示。
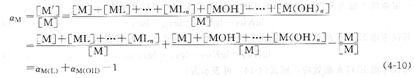
一般地,若溶液中有n个辅助配位剂能与金属离子发生副反应,则M的总副反应系数aM为:
aM=aM(L1)+aM(L2)十…+aM(Ln)一(n-1)
上式中,L也可以代表OH-所参与的羟基配位效应。
四、条件稳定常数
在配位滴定法中,如果没有副反应,溶液中M和EDTA的主反应进行的程度用稳定常数KMY表示。KMY值越大,形成的配合物越稳定。但是在实际反应中总会存在一些副反应,对主反应就会有不同程度的影响,KMY就不能客观地反映主反应进行的程度。因此,需要对式(4―3)表示的配合物的稳定常数进行修正。若仅考虑EDTA的副反应(酸效应和共存离子效应)和金属离子的配位效应的影响,则得到下式:
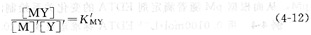
式中,[M]’和[Y]’分别表示M和Y的总浓度;K,MY称为条件稳定常数,它是考虑了酸效应和配位效应后EDTA与金属离子配合物的实际稳定常数。采用K’MY能更正确地判断金属离子和EDTA的配位情况。
从副反应系数定义可得:
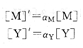
将上述关系式代入式(4―12)中,得到:
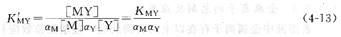
在一定条件下(如溶液的pH和试剂浓度一定时),aM和aY均为定值,因此,K’MY在一定条件下也为常数。用对数形式表示,则式(4 13)可以表示为:
lgK’MY二lgKMY―lgaM―lgaY
若仅考虑EDTA酸效应和金属离子的配位效应,则式(4―14)可表示为:
LgK’MY=lgKMY―lgaM―lgaY(H)
若仅考虑EDTA酸效应,则式(4―14)可表示为:
LgK’MY=lgKMY―lgaY(H)
参考资料:分析化学







