首页>技术中心>技术资讯>定量分析中的分离方法及一般分析步骤(二)
定量分析中的分离方法及一般分析步骤(二)
发布时间:2017-09-01
2、常用螯合剂
金属离子与螯合剂(亦称萃取配合剂)的阴离子结合形成中性螯合物分子。这类金属螯合物难溶于水而易溶于有机溶剂,因而能被有机溶剂所萃取,如丁二酮肟。常用的螯合剂还有8-羟基喹啉、双硫腙、乙酰丙酮和噻吩甲酰三氟丙酮(TTA)等。
三、离子交换分离法
利用离子交换剂与溶液中的离子发生交换作用使离子分离的方法,称为离子交换分离法。
(一)离子交换树脂
离子交换树脂是具有网状结构的复杂有机高分子聚合物。网状结构的骨架部分一般很稳定,不溶于酸、碱和一般溶剂。在网状结构的骨架上有许多可被交换的活性基团。根据活性基团的不同,离子交换树脂可分为阳离子交换树脂和阴离子交换树脂两大类。
1、阳离子交换树脂
阳离子交换树脂含有酸性基团,如应用最广泛的强酸性磺酸型聚苯乙烯树脂,它是以苯乙烯和二乙烯苯聚合,经浓硫酸磺化而制得的聚合物。这种树脂的化学性质很稳定,具有耐强酸、强碱、氧化剂和还原剂的性质,因此应用非常广泛。
各种阳离子交换树脂含有不同的活性基团,常见的有磺酸基(一SO2H)、羧基(-COOH)和酚基(-OH)等。根据活性基团离解出H+能力的大小不同,将阳离子交换树脂分为强酸性和弱酸性两种。例如,含一SO3H的为强酸性阳离子交换树脂,常用R―SO3H表示(R表示树脂的骨架脂,分别用R-COOH和R―OH表示。交换反应为:
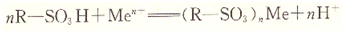
式中,Men+代表阳离子。
这种交换反应是可逆的,已交换的树脂用酸处理时,反应便向相反方向进行,树脂又恢复原状,这一过程为“再生过程”,亦称洗脱过程。
强酸性阳离子交换树脂应用较广泛,弱酸性阳离子交换树脂的H+不易锯离,所以在酸性溶液中不能应用,但它的选择性较高而且易洗脱。
2、阴离子交换树脂
阴离子交换树脂与阳离子交换树脂具有同样的有机骨架,只是所联的活性基团为碱性基团。如含季胺基(-N+(CH3)3)的树脂称为强碱性阴离子交换树脂,含伯胺基(-NH2)、仲胺基(-NHCH3)和叔胺基(一N(CH3)2)的树脂为弱碱性阴离子交换树脂。这些树脂水化后分别形成 R-NH3OH, R―NH 2 CH。OH,R―NH(CH3)2OH 和R-N(CH3)3OH等氢氧型阴离子交换树脂,所联的OH-能被阴离子交换。交换和洗脱过程可表示为:

阴离子交换树脂的化学稳定性及耐热性能都不如阳离子交换树脂。
(二)离子交换分离的操作方法
在分析工作中,为了分离或富集某种离子,一般采用动态交换,这种交换方法在交换柱中进行。其操作过程如下:
1、树脂的选择和处理
在化学分析中应用最多的为强酸性阳离子交换树脂和强碱性阴离子交换树脂。生产上出厂的交换树脂颗粒大小往往不够均匀,故使用时应当先过筛以除去太大及太小的颗粒,也可以用水泡胀后用筛在水中选取大小一定的颗粒备用。
一般商品树脂都含有一定量的杂质,所以在使用前必须进行净化处理。对强碱性和强酸性阴阳离子交换树脂,通常用4 mol/L的盐酸溶液浸泡1~2 d,以溶解各种杂质,然后用蒸馏水洗涤至中性。这样就得到在活性基团上含有可被交换的H+或C1-的氢型阳离子交换树脂或氯型阴离子交换树脂。如果需要钠型阳离子交换树脂,则用硫酸处理氯型阴离子交换树脂,这一过程称为转型。转型之后亦需再用蒸馏水洗净。
2、离子交换柱的准备
离子交换通常在离子交换柱中进行。离子交换柱一般用玻璃制成,装置交换柱时,先在交换柱的下端铺上一层玻璃丝,灌入少量水,然后倾人带水的树脂,树脂就下沉形成交换层,再盖上一层玻璃丝。由于交换层的上端比溶液的流出口低,这样就可使交换层浸在液面下而不致使溶液流空。交换柱装好以后,再用蒸馏水洗涤,关上活塞,备用。应当注意,不能使树脂露出水面,因为树脂露于空气中,当加入溶液时,树脂间隙中会产生气泡,而使交换不完全。
交换柱也可以用滴定管代替。
3、交换过程
将试液加到交换柱上,用活塞控制一定的流速进行交换。经过一段时间之后,上层树脂全部被交换,下层未被交换,中间则部分被交换,这中间的一段称为“交界层”。如果以“+”表示已交换的树脂,以“。”表示未被交换的树脂,随着交换的进行,交界层逐渐下移,至流出液中开始出现被交换离子时,称为始漏点(亦称泄漏点或突破点),此时交换柱上被交换离子的毫克当量①数称为始漏量。在到达始漏点时,交界层的下端刚到达交换柱的底部,而交换层中尚有未交换的树脂存在,因此始漏量总是小于总交换量。
4、洗脱过程
当交换完毕之后,一般用蒸馏水洗去残存溶液,然后用适当的洗脱液进行洗脱。在洗脱过程中,上层被交换的离子先被洗脱下来,经过下层未被交换的树脂时,又可发再度被交换。因此,最初洗脱液中被交换离子的浓度等于零。随着洗脱的进行,洗出液中离子浓度逐渐增大,达到最大值之后又逐渐减小,至完全洗脱之后,被洗出之离子浓度又等于零。取V1~V2一段体积的溶液,即可测定被交换离子的含量。对于阳离子交换树脂常采用盐酸溶液作为洗脱液,经过洗脱之后树脂转为氢型;阴离子交换树脂常用氯化钠或氢氧化钠溶液作为洗脱液,经过洗脱液洗脱之后,树脂转为氯型或氢氧型。因此,洗脱之后的树脂已得到再生,用蒸馏水洗涤干净即可再次使用。
四、液相色谱分离法
液相色谱分离法又称层析分离法,这种方法是由一种流动相带着试样经过固定相,物质在两相之间进行反复的分配,由于物质在两相之间的分配系数不同,移动速度也不一样,从而达到互相分离的目的。液相色谱分离法有多种类型,按其操作的形式不同,可分为柱中色谱法、纸上色谱法和薄层色谱法等。
(一)柱中色谱法
柱中色谱法是把吸附剂(如氧化铝、硅胶等)装在一支玻璃管中,做成色谱柱。然后将试液加在柱上,如试液中含有A与B两种组分,则A和B便被吸附剂(固定相)吸附在柱的上端,再用一种洗脱剂(亦称展开剂)进行冲洗。由于各种物质在吸附剂表面上具有不同的吸附选择性和吸附牢度,所以在用展开剂冲洗过程中,管内就连续不断地发生溶解、吸附、再溶解、再吸附的现象。由于展开剂与吸附剂二者对A和B的溶解能力和吸附能力不同,即A与B的分配系数不同,则A和B的移动距离也不相同。当冲洗到一定程度时,两者即可以完全分开,形成两个带。再继续冲洗,A物质便从柱中流出来,承接于一个容器中,B物质后被洗脱下来,可用另一容器承接,这样便可将A与B两种物质分离。
色谱分离法的机理可由溶质在流动相和固定相之间的分配过程来讨论。分配进行的程度可用分配系数D表示,即:
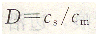
式中:cS――溶质在固定相中的浓度;
cm――溶质在流动相中的浓度;
D――分配系数,在低浓度和一定温度时是一个常数。
当吸附剂一定时,D的大小决定于溶质的性质。D大的物质被吸附得牢固,移动速度慢,在冲洗时最后洗脱下来;D=0的物质不被吸附,将随同流动相迅速流出。各组分之间的D差别越大,越容易彼此分离。各种物质对于不同的吸附剂和展开剂和展开剂有不同的D,因此,为了达到完全分离的目的,必须根据被分离物质的结构和性质(极性)选择及样度,适宜的吸附剂和展开剂。
对吸附剂的基本要求:(1)具有较大的吸附表面和一定的吸附能力;(2)与展开剂及样品中各组分不起化学反应,在展开剂中不溶解;(3)吸附剂的颗粒要有一定的细度,并且粒度要均匀。常用的吸附剂有氧化铝、硅胶、聚酰胺等。
展开剂的选择与吸附剂吸附能力的强弱和被分离物质的极性大小有关。应用吸附性弱的吸附剂分离性较大的物质时,则选用极性较大的展开剂容易洗脱;应用吸附性强的吸附剂,分离极性较小的物质时,则选用极性较小的展开剂容易洗脱。
常用的展开剂极性大小次序为:
水>乙醇>丙酮>正丁醇>乙酸乙酯>氯仿>乙醚>甲苯>苯>四氯化碳>环己烷>石油醚
以上只是一般的规则,在工作中还必须通过实验来选择合适的吸附剂和展开剂,并确定其他分离条件。
参考资料:分析化学







