滴定分析法概论
发布时间:2017-09-01
滴定分析法是定量化学分析中最重要的分析方法之一,在分析检测中应用很广,主要用在常量分析中,适用于常量组分的测定,其准确度较高,通常相对误差RE≤±0.2%。
滴定分析法是将已知准确浓度的试剂溶液通过滴定管滴加到待测组分溶液中,直到两者恰好完全定量反应为止,然后根据所加试剂的浓度和消耗的体积,计算待测组分的含量。
一、滴定分析法的术语
标准溶液:已知准确浓度的溶液,又叫滴定剂或定规液。
滴定:将标准溶液通过滴定管滴加到被测物质溶液中的操作过程称为滴定。
化学计量点:当标准溶液与被测物质恰好完全定量反应时称为化学计量点,此时正好符合化学反应式的计量关系,化学计量点又叫理论终点。
滴定终点:在滴定过程中,因指示剂颜色发生明显变化或用仪器指示而停止滴定时称为滴定终点。
终点误差:在实际分析中滴定终点与理论终点(即化学计量点)往往不可能完全一致,由此而引起的误差称为终点误差,终点误差用Et表示,是滴定分析方法误差的主要来源,又称滴定误差,它的大小取决于所用方法的化学反应平衡常数K和所选用的指示剂。
辅助试剂:为保持化学反应在一定条件下进行而加入的酸、碱、缓冲溶液、掩蔽剂等。
滴定分析法要具备的条件有:滴定分析反应、标准溶液、容量仪器、指示剂等,滴定分析误差也正是来自于这几个方面,即由于滴定反应的不完全,标准溶液浓度的不准确,容量仪器的精度限制或未经校正,指示剂误差以及操作者误差等为滴定分析带来误差。
二、滴定反应的条件
适用于滴定分析法的化学反应应具备下列条件:
(1)反应必须按一定的化学反应方程式定量完成,无副反应发生,即有定量的计算关系。
(2)反应速率要快,可以正确地控制滴定终点。对于速率慢的反应,应采取适当的措施提高反应速率或者改变滴定方式。
(3)有适当的方法确定滴定终点,如指示剂法和仪器法等。
凡能满足上述要求的反应均可用于滴定分析,如果有的样品的分析不符合上述条件,可以通过采取各种强化措施使其最终成为能用于滴定分析的反应,也可通过改变滴定程序的方法来进行测定。
三、商定分析法的分类
(一)按反应类型分类
1、酸碱滴定法
以酸碱反应(中和反应)为基础的滴定分析法叫酸碱滴定法。
酸碱滴定法即以标准酸溶液测定碱和以标准碱溶液测定酸的滴定分析法。
2、氧化还原滴定法
以氧化还原反应为基础的滴定分析法叫氧化还原滴定法。如高锰酸钾法、重铬酸钾法、碘量法、溴酸盐法、铈量法等。
3、配位滴定法
以配位反应为基础的滴定分析法叫配位滴定法,主要有EDTA滴定法等。
4、沉淀滴定法
以沉淀反应为基础的滴定分析法叫沉淀滴定法,如以生成难溶性银盐为基础的银量法等。
(二)按滴定方式不同分类
1、直接滴定法
用标准溶液直接滴定被测物质溶液进行测定的方法称为直接滴定法。这类滴定法必须要满足滴定条件。如果反应不能满足滴定反应条件,可以采用下述几种滴定方式进行滴定。
2、返滴定法
通常是在待测试液中准确加入适当过量的标准溶液,待反应完全后,再用另一种标准溶液返滴定剩余的第一种标准溶液,从而测定被测组分含量,这种方法称为返滴定法,也叫剩余量滴定法或回滴法。该方法适用于反应较慢、需加热、被测物为不易溶解的固体物质或直接滴定无合适的指示剂等反应。
例如,碳酸钙含量的测定采用的就是返滴定法。

3、置换滴定法
先加人适当的试剂与待测组分定量反应,生成另一种可被滴定的物质,再用标准溶液滴定反应产物,这种滴定方法称为置换滴定法。
这种方法适用于不能与标准溶液直接反应的物质或者反应中有副反应的情况等。
例如,用重铬酸钾(K2Cr2O7)标定Na2S2O3溶液的浓度,即在酸性重铬酸钾溶液中加入过量碘化钾(KI),定量析出I2,再用Na2S2O3标准溶液滴定I2,反应关系为:
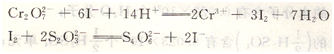
4、间接滴定法
有的被测物不能直接与标准溶液反应,但能与另一种可与标准溶液直接作用的物质反应,就可以通过反应使被测物质转换为能与标准溶液反应的物质进行滴定。这种滴定方式称为间接测定法。
例如,钙离子的测定就是采用高锰酸钾法间接测定的:
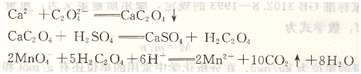
通过滴定方式的变换,更加扩展了滴定分析的应用范围。
参考资料:分析化学







