分析化学中的分离与富集方法
发布时间:2017-09-01
一、概述
在定量分析中,由于实际样品的复杂性,当测定某一组分时,不可避免存在很多干扰物质,通过适当控制实验条件或采用掩蔽法可以消除某些干扰,而分离是消除干扰最根本最彻底的方法。对于微量组分的测定,当方法灵敏度受到限制时,在分离的同时还应增大微量待测组分的浓度(富集)以提高测定的准确性。分离在定量分析中的作用体现在以下几点:①将被测组分从复杂体系中分离出来后测定;②把对测定有干扰的组分分离除去;③将性质相近的组分相互分开;④把微量或痕量的待测组分通过分离达到富集的目的。
定量分析对分离的要求是待测组分A在分离过程中的损失要小,即回收完全;干扰组分B的残留量小至不再干扰。一般用两个量化参数评价分离效果,即回收率(回收因子)和分离率(分离因子)。对待测组分A来说:
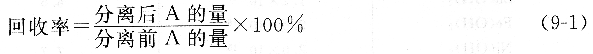
分离率用来表达A与B的分离程度:
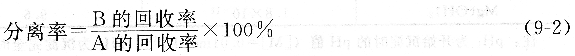
分离率越低或干扰组分B的回收率越低,A和B之间的分离越完全,干扰组分越容易消除。常量分析中,要求分离率小于10-3;痕量分析要求小于10-6。回收率越高越好,但是在分离过程中,被测组分难免有所损失。
在实际工作中,常用加入法来测回收率。对回收率的要求随被测组分的含量的不同而不同。在一般情况下,对质量分数大于1%的组分,回收率应大于99.9%;对质量分数为0.01%~1%的组分,回收率应大于99%;质量分数低于0.01%的痕量组分,回收率为90%~95%,有时更低一些也允许。
在分析化学中,常用的分离和富集方法有沉淀分离法、液-液萃取分离法、离子交换分离法、液相色谱法等,它们的共同点是都使待分离组分分别处于不同的两相中,然后用物理方法分离两相,从而将待分离物分离。如沉淀分离法涉及液相和固相,液-液萃取分离法涉及水相和有机相,离子交换分离法涉及液相(洗脱剂)和固相(树脂),液相色谱法涉及液相(流动相)和固相(固定相)两相。近年来,还出现了一些新型的分离和富集技术如固相微萃取、液相微萃取、超临界流体萃取和液膜萃取分离法等。
1、沉淀分离法
沉淀分离是一种经典的分离方法,它是根据溶度积原理,利用沉淀反应进行分离的方法。对沉淀反应的要求:所生成的沉淀溶解度小、纯度高、稳定。对于常量组分的分离,较常用的是氢氧化物沉淀分离法、硫化物沉淀分离法、硫酸盐沉淀分离法等。对痕量组分的分离富集,可采用无机沉淀剂,也可采用有机沉淀剂。
2、氢氧化物沉淀分离法
大多数金属离子都能生成氢氧化物沉淀,由于各种氢氧化物沉淀的溶度积有很大差别,因此可以通过控制溶液酸度使某些金属离子相互分离。同一浓度的不同金属离子氢氧化物开始沉淀和沉淀完全的pH不同(表9―1)。
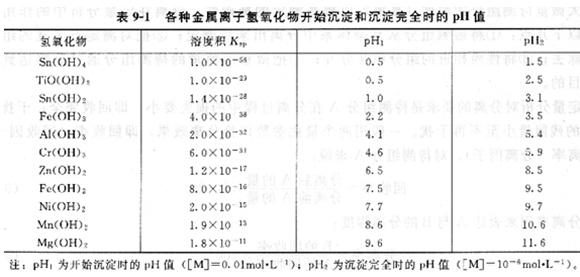
常用的沉淀剂介绍如下。
(1)氢氧化钠
NaOH是强碱,采用其作沉淀剂可使两性元素与非两性元素分离,两性元素以含氧酸阴离子形态留在溶液中,非两性元素则生成氢氧化物沉淀。一般得到的氢氧化物沉淀为胶体沉淀,共沉淀严重,所以分离效果不理想。
NaOH作为沉淀剂可定量沉淀的离子有:Mg2+、Cu2+、Ag+、Au+、Cd2+、Hg2+、Ti(Ⅳ)、Zr(Ⅳ)、Hr(Ⅳ)、Tb(Ⅳ)、Bi3+、Fe3+、C02+、Ni2+、Mn2+。
部分沉淀的离子:Ca2+、Sr2+、Ba2+、Nb(V)、Ta(V)。
溶液中存在的离子:A10-2、CrO-2、ZnO2-2、PbO2-2、SnO2-3、GeO2-3、BeO2-2、SiO2-3、WO2-4、MoO2-4、VO-3。
(2)氨缓冲溶液
在铵盐存在下,加入氨水调节和控制溶液的pH为8~9,可使高氧化值的金属离子(如Fe3+、Al3+等)与大部分低氧化值(1、2)的金属离子分离。氨缓冲溶液沉淀分离法中常加入NH4Cl等铵盐,其作用是:①控制溶液的pH为8~9,防止Mg(OH)2沉淀和减少Al(OH)。的溶解;②用NH产作为抗衡离子,减少了氢氧化物对其他金属离子的吸附;③大量存在的电解质促进了胶体沉淀的凝聚。
定量沉淀的离子:Hg2+、.Be2+、Fe3+、A13+、Cr3+、Bi3+、Sb(Ⅲ)、Sn(Ⅳ)、Mn2+、Ti(Ⅳ)、Zr(Ⅳ)、Hf(Ⅳ)、Tb(Ⅳ)、Nb(V)、Ta(V)、U(Ⅵ)。
部分沉淀的离子:Mn2+、Fe2+(有氧化剂存在时可以定量沉淀)、Pb2+(有Fe3+、Al3+共存时将被共沉淀)。
溶液中存留的离子:Ag(NH3)2+、Cu(NH3)2+4、Cd(NH3)2+4、Co(NH3)3+6、Ni(NH3)2+4、Zn(NH3)2+4、Ca2+、Sr2+、Ba2+、Mg2+。
3、硫化物沉淀分离法
硫化物沉淀分离是根据各种硫化物的溶度积相差比较大的特点,通过控制溶液的酸度来控制硫离子浓度,而使金属离子相互分离。约40余种金属离子可生成难溶硫化物沉淀,硫化氢是常用的沉淀剂,根据H2S的弱酸性,溶液中S2-的浓度与pH有关,控制溶液pH可控制分步沉淀。在进行分离时大多用缓冲溶液控制酸度,硫化物沉淀分离的选择性不高,沉淀大多是胶体,共沉淀现象比较严重,而且还存在后沉淀现象,故分离效果不理想。但利用其分离某些重金属离子还是有效的。
4、有机沉淀剂沉淀分离法
与无机沉淀剂相比,有机沉淀剂的选择性和灵敏度都较高,生成的沉淀纯净,溶解度小,易于过滤洗涤,故有机沉淀剂在沉淀分离法中的应用日益广泛,有机沉淀剂的研究和应用是沉淀分离法的发展方向。有机沉淀剂按其作用原理分为:螯合物沉淀剂、离子缔合物沉淀剂和三元配合物沉淀剂。其中,三元配合物沉淀反应相对而言,选择性和灵敏度更高,而且生成的沉淀组成稳定、相对分子质量大,作为重量分析的称量形式也更合适,近年来应用较广。
5、共沉淀分离和富集痕量组分
在重量分析中,共沉淀现象是一种消极因素,而在分离方法中,却能利用共沉淀现象来分离和富集微量组分。共沉淀分离法是在试液中加入一种试剂,使其产生一种共沉淀剂(作为载体),使被测定的组分因共沉淀作用而与共沉淀剂一同析出,以达到分离与富集的目的。
二、无机共沉淀剂
无机共沉淀剂的作用主要是通过对痕量组分的表面吸附、吸留或与痕量组分形成混晶,而把痕量组分载带下来。
(1)利用表面吸附进行共沉淀
在这种方法中,常用的共沉淀剂为氢氧化物和硫化物等胶体沉淀。由于胶体沉淀的比表面大,吸附能力强,故有利于痕量组分的共沉淀。但这种共沉淀方法的选择性不高,需选择适宜的共沉淀剂和沉淀条件才能得到较好的分离效果。
(2)利用生成混晶体进行共沉淀
该方法选择性比吸附共沉淀法高,分离效果好。常见的混晶体有:BaSO4-RaSO4,BaS04-PbSO4,MgNH4 P04 -MgN H4 As04等。
三、有机共沉淀剂
有机共沉淀剂应用较多,相对于无机共沉淀剂,它具有以下特点:有机共沉淀剂可经灼烧而除去,被测组分则被留在残渣中,用适当的溶剂溶解后即可测定;有机共沉淀剂的相对分子质量较大,体积也大,有利于微量组分的共沉淀;与金属离子生成的难溶性化合物表面吸附少,沉淀完全,沉淀较纯净,选择性高,分离效果好。有机共沉淀一般以下列三种方式进行共沉淀分离。
(1)利用胶体的凝聚作用进行共沉淀
钨、铌、钽和硅等的含氧酸常沉淀不完全,有少量的含氧酸以带负电荷的胶体微粒留于溶液中,形成胶体溶液,可用辛可宁、单宁、动物胶等将它们共沉淀下来。例如,在钨酸的胶体溶液中,可加人生物碱辛可宁,辛可宁在酸性的溶液中,其氨基被质子化而形成带正电的胶粒,能与带负电荷的钨酸胶体凝聚而共沉淀下来。
(2)利用形成离子缔合物进行共沉淀
一些分子质量较大的有机化合物,如甲基紫、孔雀绿、品红及亚甲基蓝等,在酸性溶液中带正电荷,当它们遇到以配阴离子形式存在的金属配离子时,能生成微溶性的离子缔合物而被共沉淀出来。
在这种共沉淀体系中,作为金属配阴子的配位体的有Cl一、Br-、I一、SCN一等;被共沉淀的金属离子有Zn2+、In(Ⅲ)、Cd2+、Hg2+、Bi3+、Au(Ⅲ)、Sb(Ⅲ)等。
(3)利用惰性共沉淀剂
Ni2+与丁二酮肟生成螯合物沉淀,但当Ni2+含量很低时,丁二酮肟不能将其沉淀出来,若再加入丁二酮肟二烷酯的乙醇溶液,因丁二酮肟二烷酯难溶于水,则在水溶液中析出并将Ni2+与丁二酮肟的螯合物共沉淀下来。丁二酮肟二烷酯与Ni2+及其螯合物都不发生反应,故称这类载体为“惰性共沉淀剂”,常用的还有酚酞、a-萘酚等。对于惰性共沉淀剂的作用,可理解为利用“固体萃取剂”进行沉淀,即先将无机离子转化为疏水性化合物,再根据相似相溶的原则使其进入结构相似的载体,将疏水化合物载带下来,进而达到分离的目的。
参考资料:分析化学







