离子色谱法(三)
发布时间:2017-09-01
四、电导检测器
在介绍的HPLC检测技术同样适用于离子色谱。在此,仅介绍离子色谱中通用的电导检测器(CD)。
1、非抑制型电导检测器
在离子色谱中,分析对象和所使用的流动相都是离子性物质,不同的离子其溶液的导电性是不同的。可以用极限摩尔电导来衡量离子的导电能力(见表13.2)。流动相中主要是淋洗离子和与之平衡的反离子,其电导值称为背景电导。进样前,流动相中淋洗离子占领固定相中的离子交换位置。
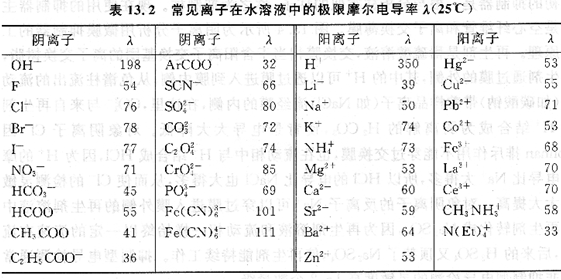
非抑制型离子色谱使用的是低电导的流动相,如浓度为几毫摩尔每升的有机酸或有机酸盐溶液,从色谱柱流出的溶液直接进入电导检测器。当样品加入后,样品带随流动相到达色谱柱,被测物质在交换基团上与淋洗离子竞争,达到最初的离子交换平衡,被交换下来的淋洗离子和被测离子的反离子迅速通过色谱柱到达检测器,在色谱图上出现一个称作“水跌”(water dip)的色谱峰(也称水峰)。各种被测物在色谱柱中的保留不同,依次流出色谱柱,此时流动相中被测离子的浓度增加了,同时有等物质的量(mo1)的淋洗离子交换到了固定相中,由于样品离子和淋洗离子的摩尔电导不同,这时流动相的电导就不同于背景电导,这种电导的变化就以色谱峰的形式记录下来。如果淋洗离子的摩尔电导比被测离子小,则在色谱图上出现正峰,阴离子通常是这种情况。阳离子交换色谱的流动相中的淋洗离子一般是H+,其极限摩尔电导远比一般阳离子大,所以,阳离子通常产生负峰(可以通过改变电导检测器的输出极性得到正峰)。在很多体系中,在被测离子峰之后还会出现一个“系统峰”(system.peak),是由样品溶液与流动相的组成、pH的差异以及淋洗离子在色谱柱中的保留所引起。它的出现往往给分离或定量带来负面影响,目前还无法完全消除系统峰,只能设法抑制系统峰的大小和调节系统峰的出峰位置使之对分析无干扰。
2、抑制型电导检测器
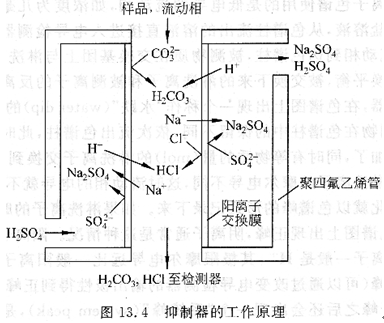
抑制型电导检测离子色谱使用的是强电解质流动相,如分析阴离子用碳酸钠、氢氧化钠,分析阳离子用稀硝酸、稀硫酸等。这类流动相的背景电导高,而且被测离子以盐的形式存在于溶液中,检测灵敏度很低,为了提高检测灵敏度,就需降低背景电导和增加被测离子的电导。分析阴离子时通常用稀硫酸(10~20mmc)l/L)作再生(抑制)剂溶液,分析阳离子时通常用稀氢氧化钠作再生剂溶液。最初的抑制器是一根与分析柱类似的柱子,称之为抑制柱。现在使用的抑制器主要是空心纤维管和离子交换薄膜。图13.4所示为阴离子分析用微膜抑制器的工作原理。再生剂是稀硫酸溶液,交换膜相当于含阳离子交换基团的离子交换树脂,再生剂通过膜的外侧,其中的H+可以透过膜进入到膜内侧,从色谱柱流出的流动相(如碳酸钠)带着样品离子(如NaCl)流经膜的内侧,在这里,CO2-3与来自再生剂的H+结合成为弱离解的H2CO3,使背景电导大大降低。对象阴离子Cl-因Donnan排斥作用不能穿过交换膜,也在流动相中与H+结合成HCl,因为H+的摩尔电导比Na+大得多,所以HaCl的电导比Na+也大得多,从而使Cl的检测灵敏度大大提高。对象阴离子的反离子Na。。可以穿过膜进入膜外侧的再生剂溶液中使再生剂转化成Na2S04,因为再生剂溶液和流动相一样始终以一定的流速在流动,后来的H2S04又顶替了Na2S04,使再生剂能持续工作。抑制型电导检测通常比非抑制型电导检测的灵敏度高1~2个数量级。
五、实验技术
1、去离子水制备及溶液配制
(1)去离子水的制备
用石英蒸馏器制得的蒸馏水的电导率在1μS/cm左右,对于高含量离子的分析,或对分析的要求不高时可以使用。作为一般性要求,离子色谱中使用的纯水的电导率应在0.5μs/cm以下。通常用金属蒸馏器制得的水的电导率在5~25μS/cm,反渗透法(RO)制得的纯水电导率在2~40μS/cm,均难以满足离子色谱的要求。因此需要用专门的去离子水制备装置制备纯水。一般是将以自来水为原水的去离子水再用石英蒸馏器蒸馏,即得到通常所说的重蒸去离子水。也可将RO水作原水引进去离子水制备装置。精密去离子水制备装置可以制得电导率O.06μS/cm以下(比电导17MΩ以上)的纯水。
2、溶液的配制
配制标准溶液时一定要防止离子污染。样品溶液和流动相配制好后要用0.5μm以下的滤膜过滤,为防止微生物的繁殖,最好现配现用。
六、流动相的选择
流动相也称淋洗液,是用去离子水溶解淋洗剂配制而成。淋洗剂通常都是电解质,在溶液中离解成阴离子和阳离子,对分离起实际作用的离子称淋洗离子,如用碳酸钠水溶液作流动相分离无机阴离子时,碳酸钠是淋洗剂,碳酸根离子才是淋洗离子。选择流动相的基本原则是淋洗离子能从交换位置置换出被测离子。从理论上讲,淋洗离子与树脂的亲和力应接近或稍高于被测离子。但在实际应用中,如果样品中强保留离子和弱保留离子共存,要是选择和保留最强的离子的亲和力接近的淋洗离子,往往有些弱保留离子很快就流出色谱柱,不能达到分离。因此,合适的流动相应根据样品的组成,通过实验进行选择。
离子抑制色谱除了控制流动相pH值外,对流动相的要求和通常的反相分配色谱一样。离子对色谱的流动相是由淋洗剂(有机溶剂或水溶液)和离子对试剂组成的。对酸性物质多用季胺盐(如溴化四甲基铵、溴化四丁基铵、溴化十六烷基三甲基铵)作离子对试剂,对碱性物质则多用烷基磺酸盐(如己烷磺酸盐、樟脑磺酸盐)和烷基硫酸盐(如十二烷基硫酸盐)作离子对试剂。离子对试剂的烷基链越长,生成的离子对化合物的疏水性越强,在固定相中的保留也随之增大,但对选择性的影响不大。所以对于性质很相似的溶质,宜选用烷基链较小的离子对试剂。离子对试剂的浓度增大,会促进离子对化合物的形成,所以也会增加被测离子的保留值。但离子对试剂的浓度超过一定的限度后溶质的保留值反而会下降,这可能是由于离子对试剂聚集在样品离子的周围增加了配合物在水相中的溶解度的缘故。所以离子对试剂有一个合适的浓度范围,较小的离子对试剂应在10mmol/L以下,较大的离子对试剂(碳链在12以上)在5mmol/L以下。
反相离子对色谱中用得最多的流动相也是甲醇一水体系,因为甲醇对许多离子对试剂有较好的溶解性。乙腈-水体系柱效也很高,但对离子对试剂的溶解性不是太好。
对分离影响较大的另一个因素是流动相的pH值,它决定被测物质的解离程度。对于硅胶基质的键合固定相,流动相的pH值应为2~8。某些缓冲剂离子也有可能与离子对试剂结合,所以缓冲剂的浓度不宜过高,通常为1~5mmol/L。
1、定性方法
当色谱柱、流动相及其他色谱条件确定后,便可根据分离机理和经验知道哪些离子在这个条件下有可能保留,而且还能根据离子的性质大致判断其保留顺序。在此基础上,就可以用标准物质进行对照。在确定的色谱条件下保留时间也是确定的,与标准物质保留时间一致就可初步认为是这种离子。这种方法称作保留时间定性法。
很多离子具有选择性或专属性显色反应,也可以用显色反应进行定性。
质谱的定性能力很强,如果离子色谱和质谱联用就可以很准确地定性。与I.C―MS联用技术一样,LC―MS联用也是在接口上存在一些困难,加上仪器昂贵,在我国尚未得到应用。
2、定量方法
在一定的被测物浓度范围内,色谱峰的高度和面积与被测离子浓度成线性关系,但一般情况下面积工作曲线的线性范围要宽一些,所以通常以峰面积的大小进行定量。IC定量方法与其他分析方法一样。用得最多的是标准曲线法(1点或多点)、标准加入法和内标法。
参考资料:现代仪器分析实验与技术







