首页>技术中心>技术资讯>动物性食品中甲硝唑、地美硝唑及其代谢物残留检测方法――超高效液相色谱一串联质谱法(一)
动物性食品中甲硝唑、地美硝唑及其代谢物残留检测方法――超高效液相色谱一串联质谱法(一)
发布时间:2017-09-01
1、安全要求
实验操作时穿工作服、戴口罩和手套;提取和净化操作都应在通风橱中进行,避免溶剂气体吸入和皮肤接触;废弃的化学试剂收集到专用容器中集中处理。
2、急救措施
皮肤接触到有机溶剂或酸、碱溶液后用清水清洗,有机溶剂或酸、碱溶液溅入眼中用清水灌洗。
3、适用范围
该标准操作规程适用于猪肌肉和猪肝脏组织中甲硝唑、地美硝唑、甲硝唑的代谢产物羟基甲硝唑、地美硝唑的代谢产物羟甲基甲硝唑残留量的确证检测。
4、职责
进行该项检验的检验员必须按该标准操作规程进行检验,质量监督员负责监督该标准操作规程正确执行。
5、检测原理
用乙酸乙酯提取试样中的硝基咪唑类药物及其代谢物,经O.1m0l/L盐酸溶液-正己烷溶液分配除脂,再经MCX固相萃取柱净化,液相色谱一串联质谱法检测,色谱保留时间和质谱碎片离子共同定性,外标法定量。
6、方法灵敏度
甲硝唑、地美硝唑、甲硝唑的代谢产物羟基甲硝唑、地美硝唑的代谢产物羟甲基甲硝唑在猪肌肉和猪肝脏组织中的检测限为0.2μg/kg,定量限为1μg/kg 。
7、注意事项
在固相萃取预洗、淋洗和洗脱过程中应注意流速,不能过快或过慢。
8、材料、仪器、试剂的准备及基本要求
除特别注明外,以下所用试剂均为分析纯;水为符合GB/T6682规定的一级水。
8.1 对照品、试剂和药物储备液、工作液准备
8.1.1 甲硝唑对照品(metronidazole,MNZ)纯度≥98%
8.1.2地美硝唑对照品(Dimetridazole,DMZ)纯度≥98%
8.1.3羟基甲硝唑对照品(Metronidazole-OH,MNZOH)纯度≥94%
8.1.4羟甲基甲硝咪唑对照品(2-Hydroxymethyl-1-methyl-5-nitro-1H-imidazole,HMMNI)纯度≥94%
8.1.5乙酸乙酯
8.1.6乙腈 色谱纯
8.1.7甲醇 色谱纯
8.1.8盐酸
8.1.9正己烷
8.1.10氨水
8.1.11 0.1mol/L盐酸溶液 取9mL浓盐酸,加水稀释至100mL。
8.1.12标准储备液的配制(100μg/mL) 精密称取甲硝唑、地美硝唑、羟基甲硝唑、羟甲基甲硝咪唑对照品各约10mg,置同一100mL棕色量瓶中,用甲醇溶解并稀释至刻度,摇匀即成浓度为100μg/mL的标准储备液。一20℃以下保存,有效期为6个月。
8.1.13标准工作液的配制(20ng/mL) 精密量取标准储备液0.1mL置10mL量瓶中,用甲醇稀释至刻度,即成1μg/mL的标准溶液;从中精密量取0.2mL,置lOmL量瓶中,用甲醇稀释至刻度,摇匀即成20ng/mL的标准工作液。一200C以下保存,有效期为6个月。
8.2仪器和设备
8.2.1超高效液相色谱-串联质谱仪(配电喷雾离子源)
8.2.2组织匀浆机
8.2.3天平 感量0.01g
8.2.4分析天平 感量0.00001g
8.2.5涡旋混合器
8.2.6振荡器
8.2.7离心机
8.2.8样品浓缩器
8.2.9旋转蒸发仪
8.2.10固相萃取装置
8.2.11 Oasis MCX固相萃取柱(60mg/3mL),或相当者
8.2.12微孔滤头0.2μm
9、检验步骤
9.1试料的制备
9.1.1 取制备后的供试样品,作为供试试料。
9.1.2取制备后的空白样品(2±0.02)g,作为空白试料(阴性对照)。
9.1.3取制备后的空白样品(2±0.02)g,添加20μg/mL的混合标准工作液0.2mL,作为空白添加试料(阳性对照)。
9.2提取
9.2.1称取供试样品(2±O.02)g置.50mL离心管中,加入乙酸乙酯15mL,涡动2min,4000r/min离心5min。
9.2.2转移上清液至100mL鸡心瓶中,残渣用乙酸乙酯15mL重复提取一次。
9.2.3合并两次提取液,400C水浴下旋蒸浓缩至干。
9.3净化
9.3.1向鸡心瓶中加入0.1mol/L盐酸3mL,涡动lmin充分溶解残渣,转移至15mL离心管中。
9.3.2 向鸡心瓶中加入正己烷3mL摇1min,转移至同一离心管中,手摇20次,4000r/min离心5min。
9.3.3弃去正己烷层,再加入0.1mol/L盐酸3mL,涡动1min。
9.3.4合并两次盐酸溶解液,加正己烷3mL重复去脂一次,除去正己烷层,备用。
9.3.5将MCX固相萃取柱置于固相萃取装置上,依次用甲醇,0.1mol/L盐酸各2mL预洗活化。
9.3.6取全部备用液在重力作用下自然流过小柱。
9.3.7再依次用O.1mol/L盐酸、甲醇、甲醇-2%氨水(10+90,v/v)各1mL淋洗,在重力下流干。
9.3.8用甲醇-5%氨水(60+40,v/v)3mL进行洗脱。
9.3.9洗脱液在40℃水浴下用氮气吹干,残余物用流动相1mL溶解,过0.2μm有机滤膜,供高效液相色谱-串联质谱仪测定。
9.4测定条件
9.4.1色谱条件
9.4.1.1 色谱柱: BEH C18(50mm×2.1mm),粒径1.7μm,或相当者;
9.4.1.2柱温:30℃;
9.4.1.3进样量:10μL;
9.4.1.4流动相A:乙腈;
流动相B:水;
流动相梯度洗脱条件见表1。

9.4.2质谱条件
9.4.2.1离子源参考参数,见表2。

9.4.2.2质量分析器参考参数见表3。

9.4.2.3光电倍增器电压:650V。
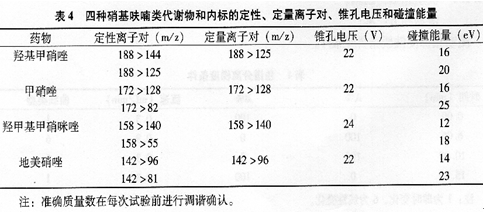
9.4.2.4定性、定量离子对、锥孔电压和碰撞能量见表4。
参考资料:兽药残留检测标准操作规程







