液相色谱分离法
发布时间:2017-09-01
色谱法又称层析法或色层分析法,是一种物理化学分离方法。其分离原理是混合物中各组分在两相之间溶解能力、吸附能力或其他亲和作用的差别,使其在两相中分配系数不同,当两相做相对运动时,组分在两相间进行连续多次分配,使得备组分被固定相保留的时间不同,从而按一定顺序由固定相中流出,实现混合物中各组分的分离。其中的一相固定不动,称为固定相;另一相是携带试样混合物流过此固定相的流体(气体或液体),称为流动相。
两相及两相的相对运动构成了色谱法的基础,色谱分析过程中总是由一种流动相带着被分离的物质流经固定相,从而使试样中的各种组分分离。按照流动相聚集态不同,色谱法可分为气相色谱和液相色谱;按固定相的形状和操作方式,可分为纸色谱、薄层色谱和柱色谱;按照被分离物质在固定相中的作用原理不同,又可分为吸附色谱、分配色谱、离子交换色谱和凝胶色谱。本节主要介绍纸色谱法和薄层色谱法。
一、纸色谱
1、分离原理
纸色谱法是以色谱用滤纸为载体的液相色谱法。分离原理一般认为是分配色谱。滤纸被看作是一种惰性载体,滤纸纤维素中吸附着的水为固定相,流动相又叫展开剂,既可用与水不相混溶的溶剂,也可用丙醇、乙醇、丙酮等与水混溶的溶剂,因为滤纸纤维素中所吸附20%~26%的水分中有6%左右通过氢键与纤维素上的羧基结合成复合物,故这部分水与和水相混溶的溶剂仍能形成类似不相混溶的两相。
将试样点在滤纸的一端,并将该端浸在展开剂中(图9―3),由于毛细作用,流动相自下而上不断上升,经过试样点时,带动试样向上运动,被分离的各组分将在固定相(水相)和流动相(有机相)之间不断进行分配和再分配,分配比大的组分上升得快(图9―4,B组分),分配比小的组分上升得慢(图9―4,A组分),从而不同组分将会得到分离。如果这些组分显色,将会在滤纸上显现出若干个分开的色斑。

比移值在纸色谱分离法中,通常用比移值(Rf)来衡量各组分分离情况。Rf的定义为:组分的迁移距离与展开剂的迁移距离之比称为比移值(图9―4)。
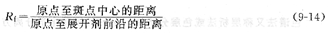
由于组分被保留在滤纸上,它的移动距离总是小于展开剂的移动距离,因此,Rf总是小于1;如果Rf=0,则该组分不溶于展开剂,留在原点不动,分配比小;Rf=1,该组分不溶于固定相(水),不被固定相保留,随溶剂前沿一起移动,分配比大。
比移值是纸色谱的基本定性参数,它说明组分在色谱系统中的保留行为。Rf大小与组分性质、流动相及溶解度有关。极性组分易保留在固定相中,其Rf小,且随流动相极性增强,Rf增大;非极性组分易流出,其Rf大,且随流动相极性增强,Rf减小。由于影响Rf的因素很多,要想得到重复的Rf,就必须严格控制色谱条件的一致性。
根据比移值的差别的大小还可以进行分离可能性的判断,两组分的Rf值差别越大,分离效果越好,一般认为两组分的△Rf>0.02,两组分即可得到完全分离。
2、操作方法
(1)滤纸的选择要求
用于色谱分离的滤纸必须具备下述条件:①质地和厚薄必须均匀,边缘整齐,平整无折痕,无污渍,不与试样组分和吸附剂发生化学反应;②纸纤维疏松度适当,过于疏松易使斑点扩散,过于紧密则流速太慢;③有一定的强度,不易断裂;④纯度高,不含填充剂,灰分在O.01%以下,否则金属离子杂质会与某些组分结合,影响分离效果。
(2)点样
溶解样品的溶剂、点样量和正确的点样方法对获得好的分离非常重要。溶解样品的溶剂最好用与展开剂极性类似的溶剂,尽量使点样后溶剂能迅速挥发,以减小色斑的扩散。适当的点样量,可使斑点集中,点样量过大,易拖尾或扩散,点样量过少,不易检出。点样时可用管口平整的玻璃毛细管或微量注射器,一张滤纸条可并排点上数点试液,两点试液间应相距一定距离,原点愈小愈好,一般直径以2~3mm为宜。
(3)展开剂的选择
展开剂的选择主要根据被分离物质的极性。一般先选择单一溶剂,但对难分离组分,则需使用二元或三元溶剂(有机溶剂、酸和水),通过比例调节展开剂的极性,改善分离效果。
展开剂各组分间以及它们与分离的物质问都不应发生反应;选择的展开剂应使待测组分在两相间迅速达到分配平衡。
(4)展开方法
一般用普通的竖式展开槽采用上行法展开,用培养皿可作径向展开,还可采用下行展开法和二向展开法等。展开时,应将展开槽密封,防止溶剂挥发。
(5)显色
对于有色物质,展开后即可直接观察到各个色斑。对于无色物质,应用各种物理的和化学的方法使之显色。由于很多有机化合物在紫外照射下,显现其特有的荧光,故可在紫外光照射下,用铅笔画出荧光斑点,或用化学显色法喷以适当的显色剂如茚三酮正丁醇溶液、Fecl3水溶液等,也可以用碘蒸气熏。注意的是,显色之后应立即用铅笔画出各色斑点的位置,以免褪色或变色后不易寻找。
3、应用
纸色谱法试样用量少,操作简便,分离效果好,常应用于有机物的分离。例如:葡萄糖、麦芽糖和木糖混合糖类的分离,可采用正丁醇:冰醋酸:水=4∶1∶5(体积比)为展开剂,用硝酸银氨溶液喷洒,即出现Ag的褐色斑点。其中,葡萄糖的Rf为0.16,麦芽糖的Rf为O.1l,木糖的Rf是0.28,由Rf值可判断是哪种糖。又如甘氨酸、丙氨酸和谷氨酸混合氨基酸的分离,采用的展开剂为:正丁醇∶冰醋酸∶水=4∶1∶2(体积比),用茚三酮显色。
4、薄层色谱分离法特点
薄层色谱分离法是将固定相吸附剂均匀地涂在玻璃上制成薄层板,试样中的各组分在固定相和作为展开剂的流动相之间不断地发生溶解、吸附、再溶解、再吸附的分配过程。不同物质上升的距离不一样而形成相互分开的斑点从而达到分离。
相对于纸色谱,薄层色谱具有以下特点:①快速,展开的时间短。一般纸色谱需要几小时至几十小时,薄层色谱一般只需十几分钟或几十分钟。②使用无机吸附剂如硅胶做固定相,可以采用腐蚀性的显色剂,如浓硫酸、浓盐酸和浓磷酸。对于特别难以检出的化合物,可喷以浓硫酸,然后小心加热,使有机物碳化,显棕色斑点,而纸色谱则无法检出。③广泛地选用各种固定相,比纸上色谱有显著的灵活性。④纸色谱法斑点的扩散作用严重,降低了单位面积中样品的浓度,降低检出灵敏度。薄层色谱法扩散作用较少,斑点比较密集,检测灵敏度较高。⑤薄层色谱法适于分析小量样品(一般几微克到几十微克),也适于大量样品的分离(可以分离出几毫克甚至几十毫克组分)。
5、固定相和展开剂的选择
薄层色谱中,固定相的选择十分重要。常用的固定相吸附剂如下:
(1)硅胶
薄层用的硅胶粒度为10~40μm。不含黏合剂的硅胶称硅胶H,硅胶中加入10%~15%煅石膏作黏合剂称硅胶G。若在硅胶G中加入荧光物质称硅胶GF254或硅胶GF254+364,表示在254nm或365nm紫外光下呈强烈黄绿色背景,适用于本身不发光又无适当显色剂显色的物质;最常用的是硅胶GF254。硅胶是一种微酸性极性固定相,适用于酸性、中性物质分离;在展开剂中加入少量酸或碱,可改变硅胶的酸碱性质,适合各种物质的分离。
(2)氧化铝
氧化铝与硅胶类似,有氧化铝H、氧化铝G、氧化铝HF254。氧化铝是一种碱性极性固定相,适用于碱性、中性物质分离,也可以制备成中性或酸性氧化铝,扩大使用范围。
(3)聚酰胺
含有酰氨基极性固定相,适用于酚类、醇类化合物的分离。
(4)纤维素
含有羟基的极性固定相,适用于分离亲水性物质。
在薄层色谱法中,展开剂的选择主要根据被分离物质的极性、吸附剂的活性以及展开剂本身的极性来决定。一般根据“相似相溶”原则来选择展开剂,因此,分离极性大的物质应选择极性大的溶剂作展开剂,分离极性小的物质应选择极性小的溶剂作展开剂。
常用的展开剂极性顺序依次为:石油醚<环己烷<四氯化碳<苯<甲苯<乙醚<氯仿<乙酸乙酯<正丁醇<丙酮<乙醇<甲醇<水。
吸附剂和展开剂的一般选择原则是:非极性组分的分离选用活性强的吸附剂。用非极性展开剂;极性组分的分离。选用活性弱的吸附剂,用极性展开剂。实际工作中要经过多次实验来确定。
6、操作方法
薄层色谱操作包括薄层板的制备、点样、展开、显色,后三种操作类似于纸色谱,在此只对薄层板的制备进行简述。
薄层色谱中多用玻璃板作为载板,要求表面光滑、平整清洁,玻璃板的大小一般有4cm×20cm、10cm×20cm、2.5cm×7.5cm等不同规格。可直接将吸附剂置于玻璃板上,涂铺成均匀薄层,但薄层易被吹散;现一般是将吸附剂与适量水研磨成稀糊状,用玻璃棒涂布成一均匀薄层。薄层的厚度一般以250μm为宜,若要分离制备少量的纯物质,薄层厚度应稍大些。铺好的硅胶板在自然晾干后,需在105~110℃温度下活化0.5~1h,然后再用。
7、应用
薄层色谱分离效果好、灵敏度高、分离快速、显色方便,应用范围非常广泛。
参考资料:分析化学







