紫外-可见吸收光谱法
发布时间:2017-09-01
紫外-可见吸收光谱法是分子吸收光谱方法,是利用分子对外来辐射的吸收特性建立起来的分析方法,是基于分子内电子跃迁产生的吸收光谱进行分析的一种方法,波长范围在180~780nm之间。
紫外-可见吸收光谱法具有许多特点,主要用于分子的定量分析,在有机化合物定性鉴定中,也是一种重要的辅助工具。紫外-可见吸收光谱法具有灵敏度高,准确度较好,仪器价格低廉,仪器简单,操作方便等优点。使紫外一可见分光光度法在有机化学、生物化学、药品分析、食品检验、医药卫生、环境保护等各个领域中成为一种重要的检测手段。
一、方法原理
紫外-可见吸收光谱起源于分子中电子能级的变化,各种化合物的紫外-可见吸收光谱的特征也就是分子中电子在各种能级间跃迁的内在规律的体现。据此,我们可以对许多化合物进行定量分析,深入认识有机化合物的结构。
1、有机化合物的紫外-可见吸收光谱
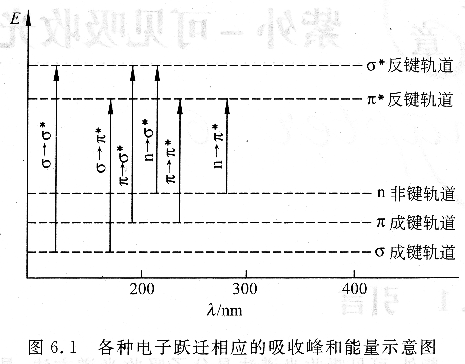
有机化合物的紫外-可见吸收光谱取决于有机化合物分子的结构。从化合物的性质来看,与紫外-可见吸收光谱有关的电子跃迁是n→σ*、n→π*和π→π*。图6.1定性地表示了各种类型的电子跃迁所需能量和吸收波长的位置。
1、n→π*σ
电子从n轨道跃迁到σ*轨道,称为n→σ*跃迁,含有杂原子S、N、O、P、卤素原子的饱和有机化合物都可以发生这种跃迁。N→σ*跃迁的大多数吸收峰出现在波长200nm以下,在紫外区不易观察到这类跃迁。
2、n→π*和π→π*跃迁
这两类跃迁一般出现在波长大于200nm的紫外区,要求有机化合物分子中含有不饱和基团,例如![]() 等,它们均含有π键的基团,称为生色团。还有一些基团并无生色作用,但有能增强生色团的生色能力,称为助色团,例如一OH、一NH2、一SH及卤素元素等,它们都含有n未成键电子。π→7*跃迁产生强吸收带,摩尔吸收系数可达104L/(mol・cm),而n→π*跃迁吸收光谱的强度小,摩尔吸收系数一般在500L/(mol・cm)以下。
等,它们均含有π键的基团,称为生色团。还有一些基团并无生色作用,但有能增强生色团的生色能力,称为助色团,例如一OH、一NH2、一SH及卤素元素等,它们都含有n未成键电子。π→7*跃迁产生强吸收带,摩尔吸收系数可达104L/(mol・cm),而n→π*跃迁吸收光谱的强度小,摩尔吸收系数一般在500L/(mol・cm)以下。
如果有机化合物含有几个生色团,生色团之间由单键分子分开,不产生共轭效应,该化合物的吸收光谱基本上由这些生色团的吸收带所组成。如果有机化合物中含有多个相同的生色团,其吸收峰的波长基本不变,而摩尔吸收系数将随生色团数目而增加。如果有机化合物分子中生色团发生共轭作用,则原有的吸收峰将发生位移,同时摩尔吸收系数增大。
当有机化合物处于气体状态时,它的吸收光谱是由孤立的分子给出,因而其振动光谱和转动光谱的精细结构也能表现出来。当有机化合物溶解于某种溶剂时,该有机物分子被溶剂分子所包围,限制了分子的自由转动,使转动光谱表现不出来。如果溶剂的极性很大,该分子的振动光谱也将消失。此外,溶剂的极性不同,也将使吸收光谱的位置发生移动。极性较大的溶剂,一般会使π一π*跃迁谱带向长波方向移动,称为红称;而使n―π*跃迁谱带移向短波方向,称为蓝移。某些有机化合物在引入含有孤对电子基团后,吸收光谱也会发生红移或蓝移。
参考资料:现代仪器分析实验与技术







