重铬酸钾法
发布时间:2017-09-01
方法概述:
K2Cr207是常用的氧化剂之一,它具有较强的氧化性,在酸性介质中Cr2O2-7一被还原为Cr3+,其电极反应如下:
Cr202-7+14H++6e-=12Cr3++7H20
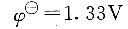
重铬酸钾的氧化能力不如高锰酸钾强,因此重铬酸钾法可以测定的物质不如高锰酸钾法广泛,但与高锰酸钾法相比,有其自己的优点。
①? K2Cr207易提纯,符合基准物质的条件,在140~1500C干燥2h后,可直接称量配制标准溶液。K2Cr2O7标准溶液相当稳定,保存在密闭容器中,浓度可长期保持不变。
②室温下,当HCl溶液浓度低于3mol・L一1时,Cr202一7不会诱导氧化C1-,因此K2Cr207法可在盐酸介质中进行滴定。
但是,Cr2O2-7的还原产物是Cr3+,呈绿色,滴定时须用指示剂指示滴定终点。常用的指示剂为二苯胺磺酸钠。
(1)铁矿石中全铁量的测定
重铬酸钾法是测定矿石中全铁量的标准方法。根据预氧化还原方法的不同分为SnCl2-HgCl2法和Sncl2-Ticl3(无汞测定法)。
① SbCl2-HgCl2法 试样用热浓HCl溶解,用SnCl2趁热将FE3+。冷却后,再用水稀释,过量的SnCl2用HgCl2氧化。然后加入H2SO4-H3PO4混合酸和二苯胺磺酸钠指示剂,立即用K2Cr2O7标准溶液滴定至溶液由浅绿(Cr3+)色变为紫红色。滴定反应为:
Cr2O2-7+6Fe2+14H+=2Cr3++6Fe3++7H2O
测定中加入H3PO4的目的有两个:一是为了降低Fe3+/Fe2+电对的电极电势,使滴定突跃范围增大,让二苯胺磺酸钠变色点的电势值落在滴定的突跃范围之内;二是为使滴定反应的产物Fe3+生成无色的 [Fe(PO4)2]3-,消除Fe3+黄色干扰,以利于滴定终点的观察。
② 无汞测定法 样品用酸溶解后,以SnCl2趁热将大部分Fe3+还原为Fe2+,再以钨酸钠为指示剂,用TiCl3还原剩余的Fe3+,反应为
Fe3++Ti3+→Fe2++Ti4+
当Fe3+定量还原为Fe2+之后,稍过量的TiCl3即可使溶液中作为指示剂的氧化值为+6的W(VI)还原为蓝色的氧化值为+5的W(V)钨化合物(俗称“钨蓝”),“钨蓝”的出现表示 已被完全还原。然后滴入重铬酸钾溶液,使钨蓝刚好褪色。最后以二苯胺横酸钠为指示剂,用K2Cr2O7标准溶液滴定溶液中的 Fe2+,即可求出全铁含量。
(2)测定污水的化学耗氧量(CODcr)
用K2Cr2O7法测定的化学耗氧量用CODcr表示。CODcr是衡量污水被污染程度的重要指标,它是目前应用最为广泛的方法。其测定原理是:
水样中加入一定量的重铬酸钾标准溶液,在强酸性(H2SO4)条件下,以Ag2SO4为催化剂,加热回流2h,使重铬酸钾与有机物和还原性物质充分作用。过量的重铬酸钾,用硫酸亚铁铵标准溶液返滴定,以1,10-邻二氮菲-亚铁为指示剂。由所消耗的硫酸亚铁铵标准溶液的量及加入水样中的重铬酸钾标准溶液的量,便可计算出水样中还原性物质消耗氧的量。
参考资料:分析化学







