氧化还原滴定指示剂
发布时间:2017-09-01
在氧化还原滴定过程中,除了用电势法确定终点外,也可以用指示剂直接指示滴定终点。氧化还原滴定中常用的指示剂有以下几种类型。
1、自身指示剂
有些标准溶液或被滴定物质本身有颜色,如果反应后变成无色或颜色很浅的物质,则滴定时就无需另加指示剂。这种物质本身颜色的变化起着指示剂的作用,所以叫做自身指示剂。例如,在高锰酸钾法中,MnO-4本身显紫红色,在滴定中,MnO-4被还原为几乎无色的Mn2+,所以用KMnO4来滴定无色或浅色的还原性物质的溶液时,一般不必另加指示剂,在滴定到化学计量点时,只要MnO-4稍过量就可以使溶液显粉红色,以指示滴定终点的到达。实验证明,KMn04的浓度约为2×10-6mol・L-1时,溶液就能呈现明显的粉红色,大约相当于100mL溶液中含O.01mL O.02tool・L-1的KMn04溶液。
2、专属指示剂
有些物质本身并不具有氧化还原性,但能与滴定剂或被测物产生特殊的颜色以确定滴定的终点,称专属指示剂。例如,在碘量法中,用淀粉作指示剂。可溶性淀粉与碘(I-3)生成深蓝色的配合物,当I2被还原为I-时,蓝色消失;当I一被氧化为I2时,蓝色出现。借此蓝色的出现与消失可指示终点。该反应实际上可看作是专属反应,而且灵敏度很高,室温下,在没有其他颜色存在的情况下,可检出约5×10-6mol・L -1的I2溶液。温度升高,灵敏度降低。
3、氧化还原指示剂
这类指示剂本身是氧化剂或还原剂,它的氧化型和还原型具有不同的颜色。在滴定过程中,指示剂由氧化型转为还原型,或由还原型转为氧化型时,溶液颜色随之发生变化,从而指示滴定终点。例如用K2Cr207滴定Fe2+时,常用二苯胺磺酸钠作指示剂。二苯胺磺酸钠的还原型无色,当滴定至化学计量点时,稍过量的K2Cr2O7使二苯胺磺酸钠由还原型转变为氧化型,溶液显紫红色,因而指示滴定终点的到达。
若以In(Ox)和In(Red)分别表示指示剂的氧化型和还原型物种,并假定电极反应是可逆的,则指示剂的电极反应和能斯特方程式为:
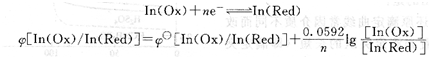
显然,随着滴定体系中电对电势值的改变,指示剂的氧化型和还原型物种的浓度比[In(Ox)/In(Red)]随之改变,溶液的颜色也发生变化。其变色与酸碱指示剂的变色情况相似。当[In(Ox)]/[In(Red)]≥10,溶液呈现氧化型物质的颜色
此时: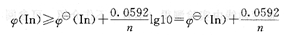
当: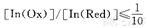 溶液呈现还原型物质的颜色,此时:
溶液呈现还原型物质的颜色,此时:
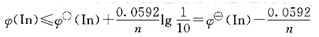
故指示剂变色的电势范围为:
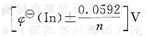
在实际工作中,考虑到离子强度和副反应,采用条件电极电势比较合适,则: